Содержимое
- 1 10. Perfluorotrimethylamine (N(CF3)3)
- 2 9. Радон (Rn)
- 3 8. Perfluorobutane (C4F10)
- 4 7. Tellurium hexafluoride (TeF6)
- 5 6. Перфторэтил йодид (CF3CF2I)
- 6 5. Decafluorodiethyl ether (C4F10O)
- 7 4. Tellurium hypofluorite (F5TeOF)
- 8 3. Iodine heptafluoride (IF7)
- 9 2. Hexamethyltungsten (W(CH3)6)
- 10 1. Tungsten hexafluoride (WF6)
- 11 Самые легкие газы
- 12 Состав воздуха
- 13 Что такое углекислый газ
- 14 Источники углекислоты
- 15 Выводы
- 16 Где используется разница массы?
- 17 Заключение
10. Perfluorotrimethylamine (N(CF3)3)
Если взять аммиак NH4 и заменить водороды на метиловые радикалы –CH3, также заменив в них водород фтором, получится перфтортриметиламин.
N(CF3)3 кипит при -6С. То есть, если вынести колбу с жидкостью на улицу, то уже при -6 градусах она начнет кипеть и испаряться. Относительная молекулярная масса газа – 221. Поделим на 29 и узнаем, что perfluorotrimethylamine тяжелее воздуха в 7,6 раз.
Какой самый тяжелый газ?
Cамый редкий и самый тяжёлый радиоактивный газ
Этот газ — радон Rn, входящий в VIIIA группу благородных газов (инертных) Периодической системы химических элементов. Радон — бесцветный газ, один литр которого имеет массу 10 г.
9. Радон (Rn)

Радон, в отличие от остальных в списке, не синтезирован человеком. Это химический элемент, занимающий 86 позицию в таблице Менделеева. Радон — почти не вступающий в реакции радиоактивный газ.
Период полураспада — 4 дня. То есть, если взять емкость с радоном и поставить в комнату, через четыре дня в колбе останется половина взятого газа. Остальная часть распадется на более легкие элементы. Да и сам радон – продукт распада радиоактивного элемента радия. Так что не стоит проделывать этот опыт, пусть он останется мысленным.
Радиоактивный радон присутствует везде: в школах, на улицах, в воздухе, почве и даже в воде. На уроках физики проводят практическую работу. Ученики спускаются в подвал и измеряют уровень радиации. Но почему в подвал?
Это связано с тем, что радон – тяжелый газ. Относительная молекулярная масса – 222. Поделив на 29, выясняем, что он тяжелее воздуха в примерно в 7-8 раз. Поскольку более тяжелое вещество опускается вниз, больше всего радона находится внизу, в подвалах и шахтах. Однако средний уровень радиации в воздухе небольшой, так что не бойтесь теперь спускаться в подвалы.
Какой газ в 1 5 раз тяжелее воздуха?
Гексафторид серы (также элегаз или шестифтористая сера, SF6) — неорганическое вещество, при стандартных условиях представляет собой тяжёлый газ (в 5 раз тяжелее воздуха).
8. Perfluorobutane (C4F10)
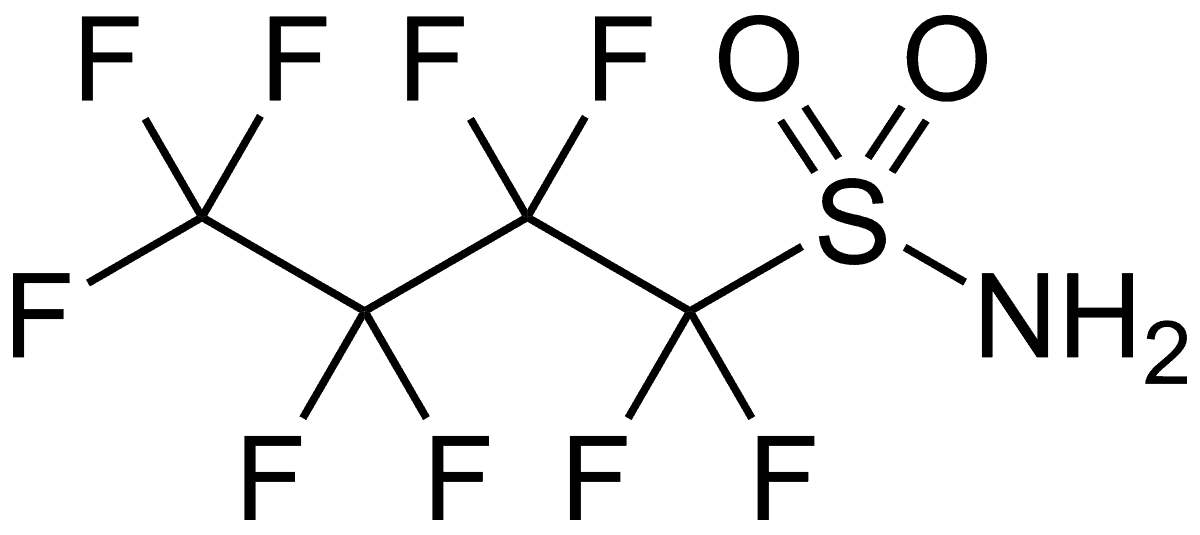
Перфторбутан – это обычный бутан C4H10, в котором атомы водорода сменили на фтор.
C4F10 – малоактивное вещество. Оно неохотно вступает в реакции, а потому не представляет угрозы организму. На него не действуют даже лучшие окислители – азотная и серные кислоты.
Перфторбутан нашел разнообразное применение. Пожарные используют газ как наполнитель для огнетушителей, врачи – как контрастное вещество для УЗИ, для инженеров это холодильный агент.
Молекулярная масса газа – 238 а.е.м. Таким образом, вещество тяжелее воздуха в 8,2 раза.
Какой газ тяжелее азот или кислород?
Угарный газ такой же как азот, легче кислорода, но тяжелее водяного пара. Если CO появляется в результате неполного сгорания, то с тёплым воздухом он уходит к потолку не успев ещё полностью размешаться. При установке под потолком несколько выше вероятность ложных срабатываний на локальные неоднородности концентрации.
7. Tellurium hexafluoride (TeF6)
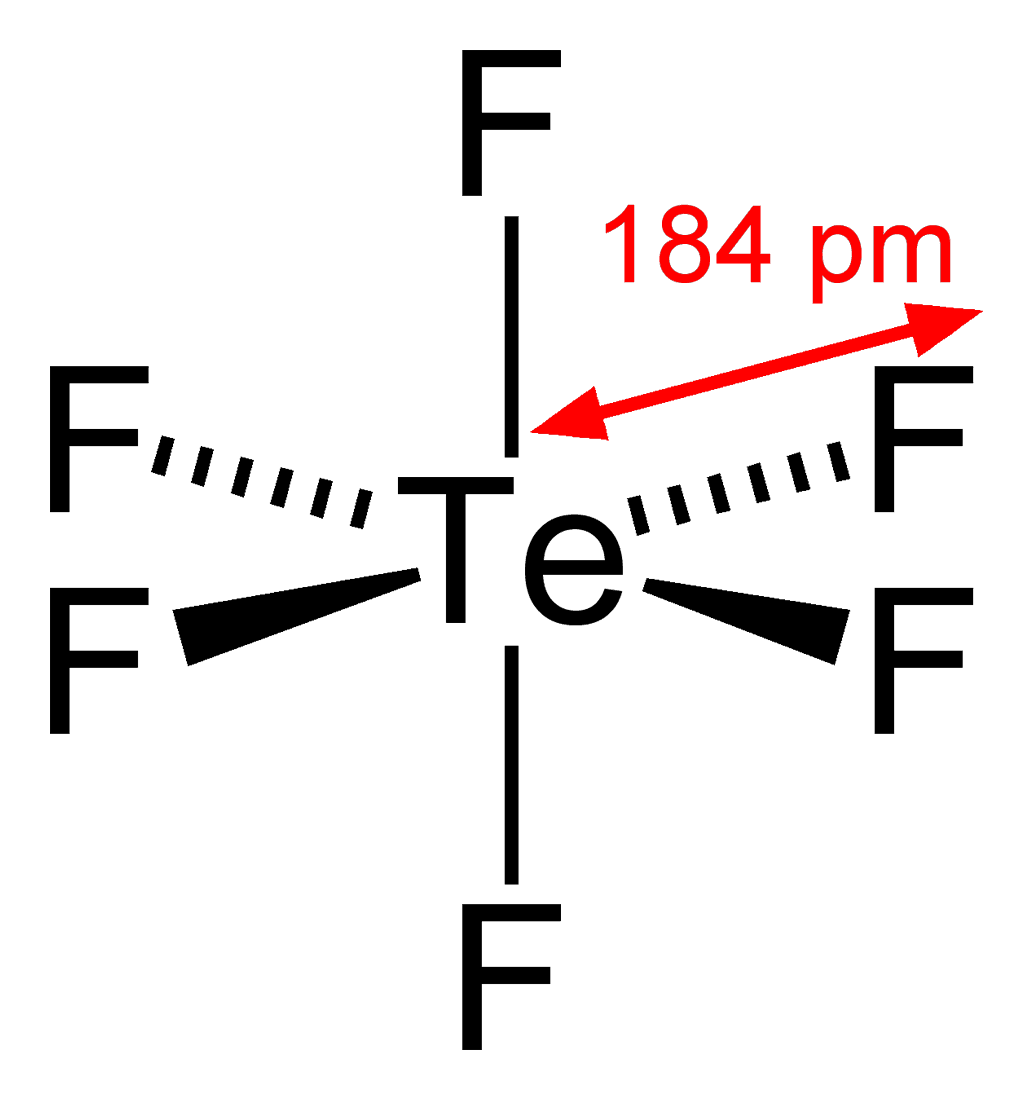
Теллур, обвешанный фтором, как новогодняя елка – это TeF6. Как и у большинства газообразных соединений теллура, у гексафторида крайне неприятный запах. Но это еще полбеды. Бесцветный газ очень токсичен и опасен для здоровья. Также реагирует с водой, разлагаясь в ней и образуя новые соединения.
Молекула весит примерно 241,6 а.е.м., а потому тяжелее воздуха в 8,33 раза.
Возможно, вы уже заметили, что в составе тяжелых газов постоянно возникает фтор. Но ведь есть элементы тяжелее фтора, почему бы не заменить водороды на них? Дело в том, что фтор – самый «агрессивный» элемент. Атому не хватает всего одного электрона для достижения баланса. Так что он с удовольствием отбирает электроны у других элементов. В молекуле легче заменить легкий водород на более тяжелый фтор – он активно вступает в реакции и утяжеляет молекулу.
6. Перфторэтил йодид (CF3CF2I)
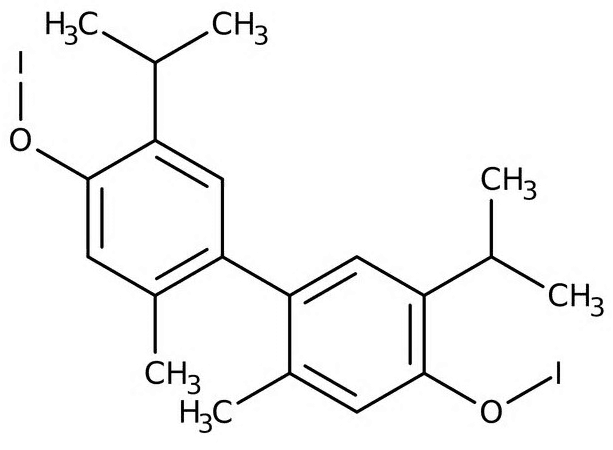
Вещество произошло от йодэтана – бесцветной жидкости, желтеющей на воздухе из-за присутствия йода. Йодэтан может быть канцерогеном, т.е. вызывать злокачественные опухоли. Также соединение обладает слабым наркотическим эффектом.
CF3CF2I – это йодэтан, в котором водород опять заменили на фтор. Вместе с изменением состава меняются и свойства вещества. Так, сообщают, что газ используют для анестезии. Значит, он уже не так вреден, как йодэтан.
Масса перфторэтид йодида – 245,9, вещество тяжелее воздуха в 8,5 раз.
Какие ядовитые газы тяжелее воздуха?
Пропан С3Н8, бутан С4Н10, пропилен С3Н6 и бутилен С4Н8 — бесцветные горючие газы, тяжелее воздуха, без запаха, трудно смешиваются с воздухом. Вдыхание пропана и бутана в небольших количествах не вызывает отравления; пропилен и бутилен оказывают наркотическое воздействие. вкусом, тяжелее воздуха.
5. Decafluorodiethyl ether (C4F10O)
Диэтиловый эфир C4H10 получили еще в IX веке, после чего открывали еще три раза. Великий хирург Н.И. Пирогов впервые стал использовать диэтиловый эфир для обезболивания во время операций. С тех пор вещество приняли как средство анестезии.
Заменив водороды на фтор, люди получили C4F10O . Скорее всего, данный эфир тоже пригоден для наркоза. Но этого никто не проверял. Относительная молекулярная масса – 254, газ тяжелее воздуха в 8,8 раз.
Как определить какой газ легче воздуха?
Ответ: Количество газов, которые легче воздуха, невелико. Способ определения того, какие газы легче или тяжелее воздуха, заключается в сравнении их молекулярного веса (который вы можете найти в списке обнаруживаемых газов).
4. Tellurium hypofluorite (F5TeOF)

Масса F5TeOF – 259,6 а.е.м., тяжелее воздуха в 9 раз. Кипит при температуре +0,6 С. Соответственно, при более низкой температуре – это жидкость. Судя по тому, что гипофторит – соединение теллура, этот газ тоже токсичен и неприятно пахнет.
Какие вещества тяжелее воздуха?
Фосген представляет собой бесцветный газ, который ниже +8,2 °C конденсируется в бесцветную жидкость. Его запах напоминает прелые фрукты или сено. Технический продукт имеет слегка желтоватую или красновато-жёлтую окраску. Фосген примерно в 3,5 раза тяжелее воздуха.
3. Iodine heptafluoride (IF7)
IF7 – бесцветный газ с резким запахом, высший фторид йода. Оба элемента I и F полностью заполнили электронные оболочки. Достигли «идеального баланса», к которому стремятся все химические элементы.
Глядя на формулу, хочется добавить в соединение хлор и получить еще более тяжелую молекулу IClF6. Однако на практике этого не выходит. Так уж получается, что нет соединений, в которых присутствует больше двух видов галогенов.
Гептафторид йода – чрезвычайно активное вещество. Это сильный окислитель, он с радостью «нападает» на металлы, а в контакте с органикой вызывает пожар. Из-за такой активности IF7 опасен для организма человека. Соединение сильно раздражает слизистые оболочки.
Газ тяжелее воздуха почти в 9 раз, молекулярная масса – 259,6 (как и у прошлого вещества из списка).
Что легче угарный газ или воздух?
Угарный газ свободно распространяется в помещении, он чуть легче воздуха. Вместе с теплым воздухом он поднимается в верхнюю часть помещения. Поскольку перемещение газа зависит от вентиляции, передвижения людей и т.
Токсичность и симптомы отравления

Нередко превышение данного показателя можно встретить в крупных городах, что разумеется, вполне возможно может, является причиной плохого самочувствия людей
Токсичность оксида углерода обусловлена его свойством образовывать стойкое соединение с гемоглобином человеческой крови. В результате происходит кислородное голодание организма на клеточном уровне. Без своевременно оказанной медицинской помощи возможны необратимые изменения в тканях и смерть.
В первую очередь страдает центральная нервная система. Повреждение нервных тканей в результате гипоксии приводит к развитию неврологических расстройств, которые могут проявиться через некоторое время после отравления.
Отравление угарным газом — острое патологическое состояние, развивающееся в результате попадания угарного газа в организм человека
Получить интоксикацию угарным газом можно в таких ситуациях:
- При пожаре в закрытом помещении.
- Химическое производство, на котором широко применяется оксид углерода.
- При использовании газовых приборов открытого типа и недостаточной вентиляции.
- Длительное нахождение на автотрассе с оживлённым движением.
- В гараже при включённом двигателе.
- При неправильном использовании печи, если заслонки закрываются раньше, чем прогорели все угли.
- Курение кальяна может вызвать симптомы отравления.
Удельный вес воздуха и угарного газа почти одинаков, но последний немного легче, благодаря чему вначале скапливается у потолка. Этим его свойством пользуются при установке датчиков, сигнализирующих об опасности. Они находятся в самой верхней точке помещения.
Очень важно своевременно распознать отравление и принять меры по спасению себя и окружающих. Есть ряд симптомов, присущих интоксикации монооксидом углерода:
- боль и тяжесть в голове;
- учащённое сердцебиение;
- увеличение давления;
- в висках слышится стук;
- своеобразный сухой кашель;
- подкатывает тошнота;
- начинается рвота;
- болевые ощущения в области груди;
- кожа и слизистые оболочки заметно краснеют;
- возможны галлюцинации.
В качестве профилактических мер во избежание отравления угарным газом следует: регулярно проверять, чистить и своевременно осуществлять ремонт вентиляционных шахт, дымоходов и отопительных приборов
Обнаружение у себя или других подобных симптомов свидетельствует о начальной стадии отравления.
Средня тяжесть характеризуется сонливостью и сильным шумом в ушах, а также двигательным параличом, при этом пострадавший ещё не теряет сознания.
Симптомы тяжёлой интоксикации:
- пострадавший теряет сознание и впадает в коматозное состояние;
- недержание мочи и кала;
- мышечные судороги;
- постоянное нарушение дыхания;
- синий цвет кожи и слизистых;
- расширение зрачков и отсутствие реакции на свет.
Человек никак не может себе помочь и смерть застаёт его на месте происшествия.
Первая помощь и лечение
Вне зависимости от степени тяжести, поражение угарным газом требует немедленной медицинской помощи. Если есть возможность самостоятельно ходить, нужно немедленно покинуть зону поражения. На пострадавших, неспособных к передвижению, надевают противогазы и срочно эвакуируют из зоны поражения.
При отравлении угарным газом необходимо сразу же вызвать бригаду скорой помощи
Первая помощь состоит из таких действий:
- Необходимо освободить человека от стесняющей одежды.
- Согреть и дать подышать чистым кислородом.
- Облучить ультрафиолетовым излучением с помощью кварцевой лампы.
- Если необходимо, проводится искусственное дыхание и массаж сердца.
- Дать понюхать нашатырный спирт.
- Как можно быстрее доставить в ближайшую больницу.
В стационаре будет проведена терапия, направленная на вывод токсина из организма. Затем проводится полноценное обследование, чтобы выявить возможные осложнения. После этого проводится ряд восстановительных мероприятий.
Чтобы избежать неприятностей и трагедий, связанных с интоксикацией, рекомендуется соблюдать нехитрые профилактические меры:

Пострадавших вследствие отравления угарным газом необходимо вывести на свежий воздух или тщательно проветрить помещение
- Следить за чистотой внутреннего просвета дымоходов.
- Всегда проверять состояние воздушных заслонок в печах и каминах.
- Хорошо вентилировать помещения с отрытыми газовыми горелками.
- Соблюдать правила безопасности при работе с автомобилем в гараже.
- При контакте с оксидом углерода принимать антидот.
Воздух тяжелее угарного газа по молярной массе на единицу. Их удельный вес и плотность мало отличаются. Монооксид углерода является губительным для человеческого организма. Статистика отравлений показывает, что пик несчастных случаев приходится на зимний период.
Свойства монооксида углерода
Угарный газ известен людям с давних времён из-за своих токсичных свойств. Тотальное использование печного отопления нередко приводило к отравлению и летальному исходу. Опасность угореть была у тех, кто прикрывал на ночь заслонку дымохода при ещё не догоревших углях в топке.
Коварство оксида углерода в том, что он не имеет цвета и запаха. Плотность угарного газа относительно воздуха немного меньше, благодаря чему он поднимается. Во время горения топлива происходит окисление углерода © кислородом (O), и выделяется углекислый газ (CO2). Для человека он безвреден и даже применяется в пищевой промышленности, при производстве газировки и сухого льда.
Данное видео расскажет вам, как выжить самому и оказать первую помощь пострадавшему в результате отравления угарным газом:
В случае, когда реакция происходит при недостаточном количестве кислорода, к каждой молекуле углерода присоединяется только одна молекула кислорода. На выходе получается CO — токсичный и горючий угарный газ.
2. Hexamethyltungsten (W(CH3)6)
Если атом вольфрама, из которого делают лампы накаливания, со всех сторон «облепить» метиловыми радикалами –CH3, получится гексаметилвольфрам.
Соединение взрывоопасно на воздухе и в вакууме. И вообще очень неустойчиво. W(CH3)6 оказалось в этом списке с натяжкой, ведь вещество распадается почти сразу после образования. Молекула весит 274,05 а.е.м, а потому тяжелее воздуха в 9,45 раз.
Что легче бутан или воздух?
Пропан, бутан или их смесь тяжелее воздуха, природный газ метан легче воздуха.
1. Tungsten hexafluoride (WF6)
Самый тяжелый газ в топе – WF6, гексафторид вольфрама. Это соль плавиковой кислоты HF и вольфрама W. Вещество газообразно при температуре выше +17 С, так что находится на грани с жидкостью. Во влажном воздухе начинает дымиться и синеть.
WF6 – коррозионно активное соединение, а также опаснейший неорганический яд. Тем не менее, газ применяют в производстве полупроводников и вольфрамовых покрытий.
Относительная молекулярная масса tungsten hexafluoride – 297.3. Газ тяжелее воздуха больше чем в 10 раз. WF6 становится рекордсменом среди самых тяжелых газов.
Самые легкие газы
Название «газ» было придумано ещё в XVII веке из-за созвучия со словом «хаос». Частицы вещества и вправду, хаотичны. Они движутся в произвольном порядке, меняя траекторию каждый раз, когда сталкиваются друг с другом. Они стараются заполнить все доступное пространство.

Молекулы газа слабо связаны между собой, в отличие от молекул жидких и твердых веществ. Большинство его видов невозможно ощутить при помощи органов чувств. Но газы обладают другими характеристиками, например, температурой, давлением, плотностью.
Их плотность увеличивается по мере возрастания давления, а при увеличении температуры они расширяются. Самым легким газом является водородом, тяжелым – гексафторид урана. Газы всегда смешиваются. Если действуют силы тяготения, то смесь становится неоднородной. Легкие поднимаются вверх, тяжелые, наоборот опускаются вниз.
Самые легкие газы – это:
- водород;
- азот;
- кислород;
- метан;
- диоксид углерода.
Водород
Какой газ является самым легким? Ответ очевиден – водород. Это первый элемент периодической таблицы, который в 14,4 раза легче воздуха. Он обозначаете буквой Н, от латинского названия Hydrogenium (рождающий воду). Водород является наиболее распространенным элементом во Вселенной. Он входит в состав большинства звезд и межзвездной материи.
В нормальных условиях водород абсолютно безвреден и нетоксичен, не обладает запахом вкусом и цветом. В определенных условиях может значительно изменять свойства. Например, смешиваясь с кислородом, этот газ запросто взрывается.

Может растворяться в платине, железе, титане, никеле и в этаноле. От воздействия больших температур он переходит в металлическое состояние. Его молекула двухатомная и обладает большой скоростью, что обеспечивает отличную теплопроводность газа (в 7 раз выше, чем у воздуха).
На нашей планете водород находится в основном в соединениях. По своей важности и задействованности в химических процессах он является вторым после кислорода. Водород содержится в атмосфере, входит в состав воды и органических веществ в клетках живых организмов.
Самый лёгкий газ
Химический элемент, молекулы которого образуют легчайший газ – это водород. В периодической системе он обозначается символом H и стоит на первом месте. Он уникален по своей природе, ведь может быть опасен, но вместе с тем он крайне необходим любому живому существу.
Водород – самый лёгкий газ, когда два его атома соединяются в молекулу, образуя H2. По легкости он превосходит воздух в 14,5 раз. В смеси с кислородом или воздухом он может взрываться. Но если соединить два его атома с атомом оксигена, то получится обыкновенная вода, в которой мы так нуждаемся. На это указывает и его латинское название Hydrogenium, что можно перевести как «порождающий воду».

Если соединить два атома водорода и два атома кислорода, то выйдет уже другое вещество. Они образуют перекись водорода – бесцветную жидкость, которую используют для обеззараживания ран, отбеливания волос, а также в качестве ракетного топлива.
Эффективное топливо
Водород обладает высокой теплотой сгорания и не представляет вред для окружающей среды Когда он горит, то в атмосферу выделяются кислород и вода. Он вполне мог бы заменить дорогие нефть и газ, тяжело добываемый уголь, а также остановить выделение вредного углекислого газа, которое неизбежно при их переработке.
Над этим вопросом сейчас и задумываются учёные. Программы по водородной энергетики уже озвучили Исландия, США, Япония, ЮАР, Индия, Южная Корея. В Италии компания Enel уже запустила электростанцию на этом газе, Япония заявила, что откроет свою станцию в 2018 году. Автомобильные компании уже давно представили свои водородные модели.
Возможно, такое топливо могло бы решить некоторые проблемы. Однако оно может породить и новые. Пока неизвестно, как эффективно получать водород, затрачивая минимум средств и не нарушая природный баланс. Поэтому все идеи об использовании самого легкого газа находятся в разработке.
Кислород
Кислород обозначается буквой О (Oxygenium). Он также не обладает запахом, вкусом и цветом в нормальных условиях, и находится в газообразном состоянии. Его молекулу часто называют дикислород, так как она содержит два атома. Существует его аллотропная форма или же модификация – газ озон (О3), состоящий из трех молекул. Он имеет голубой цвет и отличается многими характеристиками.
Кислород и водород – самые распространенные и самые легкие газы на Земле. В коре нашей планеты больше кислорода, он составляет примерно 47 % её массы. В связанном состоянии в воде его содержится больше 80 %.

Газ является важнейшим элементом жизнедеятельности растений, животных, человека и многих микроорганизмов. В теле человека он способствует осуществлению окислительно-восстановительных реакций, попадая в наши легкие с воздухом.
Благодаря особым свойствам кислорода, его широко используют в медицинских целях. С его помощью устраняют гипоксию, патологии ЖКТ, приступы бронхиальной астмы. В пищевой промышленности его применяют в качестве упаковочного газа. В сельском хозяйстве кислород используют для обогащения воды, при разведении рыбы.
Азот
Как и два предыдущих газа, азот состоит из двух атомов, не обладает выраженными вкусовыми качествами, цветом и запахом. Символ для его обозначения – латинская буква N. Вместе с фосфором и мышьяком он относится к подгруппе пниктогенов. Газ очень инертный, за что и получил название azote, которое переводится с французского как «безжизненный». Латинское название Nitrogenium, то есть «рождающий селитру».
Азот содержится в нуклеиновых кислотах, хлорофилле, гемоглобине и белках, является основной составляющей воздуха. Его содержание в гумусе и земной коре многие ученые объясняют извержением вулканов, которые переносят его с мантии Земли. Во Вселенной газ существует на Нептуне и Уране, входит в состав солнечной атмосферы, межзвездного пространства и некоторых туманностей.

Человек использует азот в основном в жидком виде. Его применяют в криотерапии, в качестве среды для упаковки и хранения продуктов. Он считается наиболее эффективным для тушения пожаров, вытесняет кислород и лишает огонь «потпитки». Вместе с кремнием он образует керамику. Азот нередко используют для синтеза различных соединений, например, красителей, аммиака, взрывчатых веществ.
Состав воздуха
Воздух, в отличие от углекислого газа, является не одним веществом, а сложнейшей смесью, в состав которой входят больше десяти веществ. И это только нормальный воздух, а не городской, в который входит еще несколько десятков опасных для человека ингредиентов.

Итак, самая большая доля приходится на азот – воздух состоит из него на 76%. Он не поддерживает горение, не используется при дыхании.
А вот следующий компонент жизненно важен всему живому – кислород. Его в составе воздуха значительно меньше, лишь 23%. Но именно он позволяет человеку, животным, птицам, рыбам и растениям жить. Да-да, растения тоже дышат, хотя это и известно не всем.
Третий газ в составе воздуха – аргон. Его уже совсем немного, лишь 1,3 процента. В живой природе он также почти не применяется, зато активно используется людьми в разных сферах деятельности.
Четвертое же место занимает именно углекислый газ. Правда, количество очень невелико – только 0,046%. Представьте себе, все заводы, автомобили и живые существа на планете почти не могут повысить этот показатель. Хотя, по прогнозам экологов, вредное производство и вырубка лесов приводят к тому, что этот показатель все-таки увеличивается.
Также воздух состоит из неона, криптона, метана, гелия, водорода и ксенона. Последний занимает всего 0,00004% от общей массы. Другие примеси настолько незначительны, что о них можно и не говорить.
Что такое углекислый газ
Оксид углерода (IV) представляет собой тяжёлый газ. Плотность углекислоты примерно в полтора раза больше чем у атмосферного воздуха. Несмотря на то, что этот газ уже при температуре минус 78,3 градуса Цельсия превращается в снегообразную массу, получить жидкую углекислоту при нормальном давлении не представляется возможным. Так называемый сухой лёд при малейшем повышении температуры сразу переходит из твёрдой, в газообразную форму. Получить жидкую углекислоту можно только при давлении более 60 атмосфер. В таких условиях газ конденсируется даже при комнатной температуре с образованием бесцветной жидкости.
Углекислый газ не окисляется, но может поддерживать горение некоторых металлов. В среде углекислоты, при определённых условиях, могут возгораться такие активные элементы как магний, кальций и барий. Этот газ хорошо растворим в воде, а в воздухе его содержится большое количество благодаря дыханию живых организмов и растений, наличию вулканической активности на земле, а также в результате сгорания органических веществ.
В результате растворения СО2 в воде в большой концентрации образуется угольная кислота. Это вещество может вступать в реакцию с фенолом и магнийорганическими соединениями. Углекислый газ также реагирует с щелочами. В результате такой реакции образуются соли и эфиры угольной кислоты.
Взаимодействие с океаном
В океанах углекислота по наличию превышает атмосферное содержание, если пересчитать на углерод, то выйдет примерно 36 триллионов тонн. 2Растворенный в океане CO находится в виде гидрокарбонатов и карбонатов. Эти соединения образуются в процессе химических реакций между подводными скальными породами, водой и двуокисью углерода. Реакции эти обратимы, они вызывают образование известняковых и других карбонатных пород с высвобождением половины гидрокарбонатов в виде диоксида углерода.
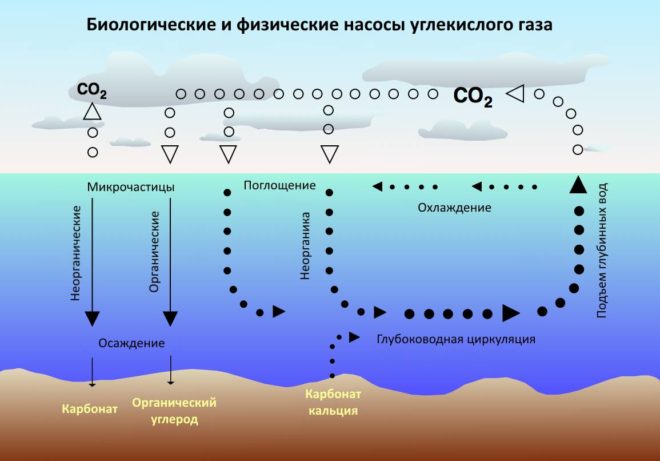
Круговорот углекислого газа в океане.
Протекая сотни миллионов лет, этот круговорот реакций привёл к связыванию в карбонатных породах большей части диоксида углерода из атмосферы Земли. По итогу большинство двуокиси углерода, полученной в результате интенсивных выбросов углекислого газа в атмосферу человеком, будет растворено в океанах. Но скорость, с которой будет протекать этот процесс в дальнейшем, остается неизвестной.
Наличие фитопланктона на поверхности океанов помогает поглощать СО2 из воздуха в океан. Некоторое количество углекислого газа фитопланктон поглощает при фотосинтезе, приобретая энергию и источник для развития клеток. Когда он погибает и спускается на дно, углерод остается с ним.
Свойства углекислого газа
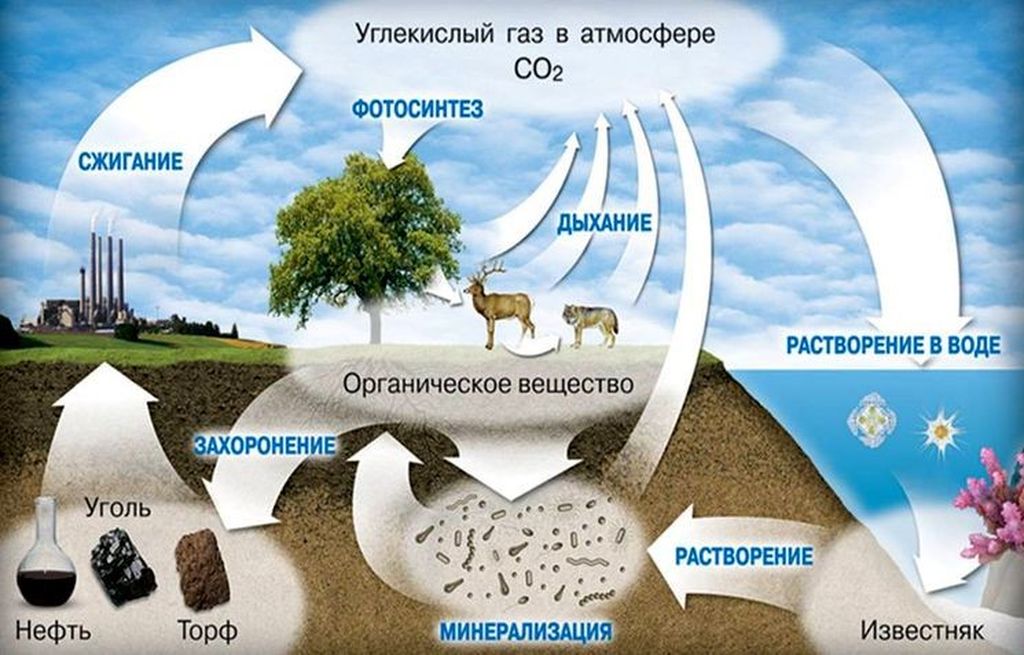
Углекислый газ невозможно определить органами зрения или обоняния. Если концентрация СО2 невелика, то не будет ощущаться и вкуса, но при наличии большого количества этого газа в воздухе может ощущаться кисловатый привкус.
При большой концентрации углекислоты во вдыхаемом воздухе может наступить отравление. Признаками негативного воздействия СО2 на организм человека являются:
- Шум и гул в ушах.
- Обильный холодный пот.
- Потеря сознания.
Учитывая тот факт, что углекислый газ тяжелее воздуха, его концентрация в нижней части помещения будет более значительной. По этой причине, первую очередь симптомы отравления могут наблюдаться у животных и детей, а также у взрослых очень маленького роста. Большая концентрация СО2 может привести к гибели людей. При потере сознания человек может оказаться на полу, где количество кислорода будет недостаточным для поддержания нормального процесса дыхания.
Нормы и правила содержания углекислого газа
В зарубежных стандартах концентрация углекислого газа в воздухе помещений служит индикатором содержания других более вредных загрязняющих веществ и по этому параметру рассчитывается вентиляция.
Европейский стандарт ЕН 13779 «Ventilation for non-residential buildings – Performance requirements for ventilation and room-conditioning systems» в качестве общего базового руководства предлагает принимать концентрацию углекислого газа в сельской местности 350 ppm, в небольших городах 400 ppm, в центрах городов 450 ppm. На самом деле она может быть существенно выше. Например, измерения в центре Москвы в безветренную погоду в конце лета в районе Садового кольца показали, что при достаточно интенсивном движении транспорта уровень СО2поднимался до 900 ppm (0,09 % об.).
Проектировщики многоквартирных и частных домов берут за основу ГОСТ 30494-2011 под названием «Здания жилые и общественные. Параметры микроклимата в помещениях». Этот документ оптимальным для здоровья человека уровнем CO2 считает 800 — 1 000 ppm. Отметка на уровне 1 400 ppm – предел допустимого содержания углекислого газа в помещении. Если его больше, то качество воздуха считается низким.
Взаимодействие с землей
Углекислый газ воздуха на генетическом уровне взаимосвязан с землей. Постоянно протекающие почвенные движения увеличивают резервы СО2 в воздухе, где он используется растениями на образование органических элементов. Углекислота выполняет важную функцию в формировании и проветривании почвы. Он принимает участие в разрушении основных минералов, увеличении растворяемости, перемещении карбонатов и фосфатов.
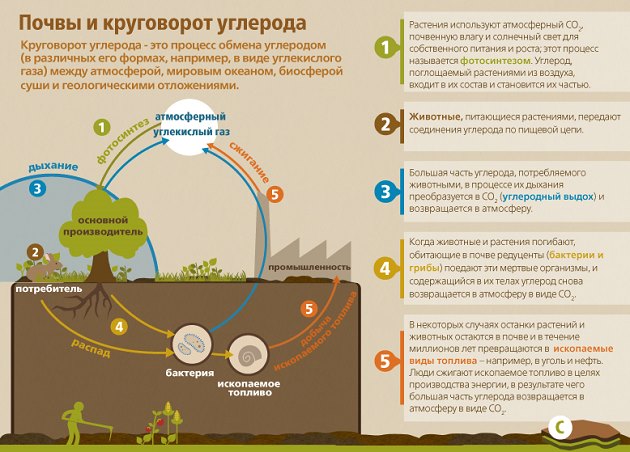
Значительная доля диоксида углерода грунтового воздуха появляется в результате деятельности почвенных организмов, во время распада и окисления органического элемента. До 1/3 части СО2 вырабатывается корнями высоких растений. Также происходит поступление углекислого газа с газами ювенильного и вадозного происхождения из глубочайших шаров земли. В почвах, сформированных на известковых породах, СО2 способен выступать продуктом разрушения углекислого кальция почвенными кислотами.
СО2 грунтового воздуха имеет огромную биологическую значимость. Ее излишек (больше 1%) подавляет проращивание семян и рост корневой системы. Если убрать углекислоту все равно ее кратковременный излишек приведет к медленному росту семян.
В почвах с большим содержанием органического вещества концентрация СО2 летом и весной увеличивается до 3-9 %. Черноземные грунты вырабатывают от 2 до 6 кг углекислого газа на протяжении 24 часов. В почвенном воздухе на глубине 75-150 см в два раза больше содержание СО2 нежели в верхних слоях. В теплые времена содержание СО2 в почвенном воздухе в два раз больше чем в зимний период. Объяснить это можно увеличением активности организмов в грунте.
Необходимо понимать, что многочисленные способы земледелия приводят к повышению концентрации углекислоты в грунте. Среди них можно выделить:
- органические удобрения;
- травосеяние;
- сжатие катками.
Безусловно, не стоит говорить, что плодородность и качество земли зависит исключительно от углекислоты, есть и другие факторы, влияющие на это.
Чтобы регулировать динамику СО2 в почве и увеличивать его содержание до требуемого количества для извлечения хорошего урожая необходимо:
- активировать жизненные процессы в грунте при помощи аэрации;
- осуществлять правильное травосеяние для того чтобы поддерживался и обновлялся резерв органического вещества;
- делать сидерацию и вносить органические удобрения.
Чем опасно повышение уровня углекислого газа
Качество воздуха зависит от наличия в нем вредных веществ и концентрации углекислого газа СО2. В отличие от угарного газа, углекислый газ нетоксичен, но при вдыхании его повышенных концентраций все живые организмы испытывают удушье.
Незначительные повышения концентрации, вплоть до 2-4 %, в помещениях приводят к развитию у людей сонливости и слабости. Люди страдают от головной боли, головокружения, расстройстве слуха и в потере сознания (симптомы, сходные с симптомами высотной болезни), эти симптомы развиваются, в зависимости от концентрации, в течение времени от нескольких минут до одного часа.
Интенсивно выделяется углекислый газ от газовой плиты при приготовлении пищи. При возрастании содержания в воздухе значения CO2 выше определенной величины человек начинает чувствовать себя дискомфортно, может впадать в дремотное состояние, возникают головные боли, тошнота, чувство удушья. Его влияние настолько постепенное и слабое, что его трудно сразу обнаружить.
Превышение уровня углекислого газа вредно для состояния организма человека, поэтому за ним необходимо следить. Для этого есть специальные датчики (газоанализаторы).
Почему важно следить именно за концентрацией углекислого газа? Потому что его много, измерить легче. Но многочисленные исследования показали, что рост содержания СО2 в помещении напрямую связан с повышением уровня и других вредных веществ (формальдегида, фенола, бензола и т.п.) — это явный признак того, что качество воздуха снижается. Ведь чем хуже вентиляция, тем больше загрязнителей концентрируется в воздухе.
Нормы углекислого газа в школах
Чем больше углекислого газа в воздухе, тем сложнее сосредоточиться и справиться с учебной нагрузкой. Зная об этом, власти США рекомендуют школам поддерживать уровень СО2 не выше 600 ppm. В России отметка чуть выше: уже упомянутый ГОСТ считает оптимальным для детских учреждений 800 ppm и менее. Однако на практике не только американский, но и российский рекомендуемый уровень – голубая мечта для большинства школ.
Один из наших экспериментов в школе показал: больше половины учебного времени количество углекислого газа в воздухе превышает 1 500 ppm, а иногда приближается к 2 500 ppm! В таких условиях невозможно сосредоточиться, способность к восприятию информации критически снижается. Другие вероятные симптомы переизбытка СО2: затрудненное дыхание, потливость, воспаление глаз, заложенность носа.
Почему так происходит? Классы редко проветриваются, потому что открытое окно – это простывшие дети и шум с улицы. Даже если школьное здание оснащено мощной центральной вентиляцией, она, как правило, либо шумная, либо устаревшая. Зато окна в большинстве школ современные – пластиковые, герметичные, не пропускающие воздух. При численности класса 25 человек в кабинете площадью 50–60 м2 c закрытым окном углекислый газ в воздухе подскакивает на 800 ppm за каких-то полчаса.
В пресс-релизе ежегодной конференции Европейского респираторного общества в 2006 году были опубликованы результаты исследований, проведенных в пяти странах ЕЭС группой итальянских ученых. Исследования показали, что 68 % детей испытывают на себе негативное влияние СО2 выше уровня 1 000 ppm. У них наблюдалось тяжелое дыхание, одышка, сухой кашель и ринит чаще, чем у других детей. Были сделаны следующие выводы: у детей, находящихся в помещении с высоким уровнем СО2, в 3,5 раза выше риск возникновения сухого кашля и в 2 раза – развитие ринита. Они имеют более уязвимую носоглотку, чем их ровесники.
В исследовании корейских ученых о влиянии концентрации СО2 в помещении на приступы астмы у детей, в домах и квартирах, где живут дети больные астмой, замерялся уровень содержания веществ, которые считаются основными загрязнителями воздуха в помещении, таких как СО, NO2, аллергены и СО2. В результате данных исследований были сделаны выводы о том, что самым важным фактором, влияющим на возникновение приступов астмы у детей, является только уровень концентрации СО2.
Источники углекислоты
Большая часть диоксида углерода планеты естественного происхождения. Но также источниками СО2 являются промышленные предприятия и транспорт, которые обеспечивают выброс в атмосферу углекислого газа искусственного происхождения.
Природные источники
При перегнивании деревьев и травы каждый год выделяется 220 миллиардов тонн углекислого газа. Океанами выделяется 330 миллиардов тонн. Пожары, которые образовались в связи с природными факторами приводят к выбросу СО2, равному по количеству антропогенной эмиссии.

Естественными источниками углекислоты являются:
- Дыхание флоры и фауны. Растения и животные поглощают и вырабатывают СО2, так устроено их дыхание.
- Извержение вулканов. Вулканические газы содержат двуокись углерода. В тех регионах, где есть активные вулканы, углекислый газ способен выходить из земных трещин и разломов.
- Разложение органических элементов. Когда органические элементы горят и перегнивают появляется СО2.
Диоксид углерода хранится в углеродных комбинациях: угле, торфе, нефти, известняке. В качестве резервных хранилищ можно назвать океаны, в которых содержатся большие резервы углекислоты и вечную мерзлоту. Однако, вечная мерзлота начинает таять, это можно заметить по уменьшению снежных шапок самых высоких гор мира. При разложении органики наблюдается рост выделения в атмосферу углекислого газа. В результате чего хранилище преобразуется в источник.
Северные районы Аляски, Сибири и Канады — это в основном вечная мерзлота. В ней содержится много органического вещества. Из-за нагрева арктических регионов вечная мерзлота тает и происходит гниение ее содержимого.
Антропогенные источники
Главными искусственными источниками CO2 считаются:
- Выбросы предприятий, которые происходят в процессе сгорания. Результатом является значительное повышение концентрации углекислого газа в атмосфере планеты.
- Транспорт.
- Превращение хозяйственных земель из лесов в пастбища и пахотные земли.

В мире растет количество экологических машин, но их процент по отношению к машинам внутреннего сгорания очень мал. Стоимость электрокаров выше обычных машин, поэтому многие не имеют финансовой возможности приобрести такой вид транспорта.
Интенсивное сокращение лесов для промышленности и сельского хозяйства относится к антропогенным источникам CO2 не в прямом смысле. Деятельность по уменьшению лесных массивов является причиной неучастия диоксида углерода в процессе фотосинтеза. Что приводит к его накоплению в атмосфере.
Выводы
В квартирах, офисных зданиях и детских образовательных учреждениях наиболее выражена проблема с вентиляцией. Она усугубляется и тем, что между строительными и санитарно-гигиеническими нормативами есть существенные расхождения. Если ГОСТ допускает превышение нормы СО2 до 1400ppm, то физиологи верхним предельным значением называют 800-1000.
На ситуацию сильно влияет и строительство с нарушениями: недостаточная вентиляция и установка пластиковых окон, кондиционеров без обеспечения соответствующего притока свежего воздуха. В помещениях, где постоянно находятся люди и невозможно постоянно держать открытыми окна, следует установить датчики контроля СО2 и компактную приточную вентиляцию, помогающую стабильно снижать уровень углекислого газа, исключая его пагубное воздействие на здоровье.
Где используется разница массы?
Зная, что тяжелее – воздух или углекислый газ, можно предположить, что последний всегда стремится вниз. И это можно использовать на практике. Например, применяется данный эффект водолазами при погружении с колпаком. Запас воздуха здесь ограничен, и, если бы углекислый газ смешивался с ним равномерно, дыхание было бы затруднено. Но его избыток преимущественно выделяется и опускается ниже, позволяя человеку легко дышать.
Применяется этот эффект и при пожаротушении. Углекислым газом заправляют специальные огнетушители – углекислотные. Когда сжиженный газ вырывается из раструба, он тут же расширяется примерно в 400-500 раз, заодно охлаждаясь на 72 градуса. Уже этого достаточно, чтобы многие горящие предметы потухли. Но тяжелый газ расползается по полу и горящим предметам, вытесняя воздух. Так как СО2 не поддерживает горение, то пламя, оставшись без подпитки кислородом, просто гаснет.
Заключение
На этом можно закончить статью. Теперь вам известно, что тяжелее – воздух или углекислый газ, и во сколько раз. Заодно вы узнали об основных свойствах обоих веществ, их важности в природе, а также использовании разницы плотности в человеческой жизни. Будем надеяться, что эта информация окажется для вас полезной.
- https://top10a.ru/samye-tyazhelye-gazy.html
- https://abckeys.ru/kakoy-gaz-tyazhelee-vozduha/
- https://abckeys.ru/chto-legche-vozduh-ili-gaz/
- https://kaminguru.com/obsluzhivanie/ugarnyj-gaz.html
- http://kamin.Spb.ru/izolyaziya/obsluzhivanie-ugarnyj-gaz/
- https://FB.ru/article/284774/samyie-legkie-gazyi-osobennosti-vodoroda-kisloroda-i-azota
- https://www.syl.ru/article/362854/samyiy-legkiy-gaz-v-mire-i-ego-harakteristiki
- https://FB.ru/article/394314/chto-tyajelee-vozduh-ili-uglekislyiy-gaz-otvet-na-vopros
- https://ballonis.ru/stati/uglekislyy-gaz-harakteristiki-i-primenenie
- https://UglekislyGaz.ru/dioksid-ugleroda/co2-v-atmosfere/
- https://safetydom.net/atmosphere/91-uglekisliy-gaz.html
- https://izmerkon.ru/podderzhka/publikaczii/normy-so2.html





